7.7: Ataque Nucleofílico por Hidruros o Carbaniones
- Page ID
- 76914
\( \newcommand{\vecs}[1]{\overset { \scriptstyle \rightharpoonup} {\mathbf{#1}} } \)
\( \newcommand{\vecd}[1]{\overset{-\!-\!\rightharpoonup}{\vphantom{a}\smash {#1}}} \)
\( \newcommand{\dsum}{\displaystyle\sum\limits} \)
\( \newcommand{\dint}{\displaystyle\int\limits} \)
\( \newcommand{\dlim}{\displaystyle\lim\limits} \)
\( \newcommand{\id}{\mathrm{id}}\) \( \newcommand{\Span}{\mathrm{span}}\)
( \newcommand{\kernel}{\mathrm{null}\,}\) \( \newcommand{\range}{\mathrm{range}\,}\)
\( \newcommand{\RealPart}{\mathrm{Re}}\) \( \newcommand{\ImaginaryPart}{\mathrm{Im}}\)
\( \newcommand{\Argument}{\mathrm{Arg}}\) \( \newcommand{\norm}[1]{\| #1 \|}\)
\( \newcommand{\inner}[2]{\langle #1, #2 \rangle}\)
\( \newcommand{\Span}{\mathrm{span}}\)
\( \newcommand{\id}{\mathrm{id}}\)
\( \newcommand{\Span}{\mathrm{span}}\)
\( \newcommand{\kernel}{\mathrm{null}\,}\)
\( \newcommand{\range}{\mathrm{range}\,}\)
\( \newcommand{\RealPart}{\mathrm{Re}}\)
\( \newcommand{\ImaginaryPart}{\mathrm{Im}}\)
\( \newcommand{\Argument}{\mathrm{Arg}}\)
\( \newcommand{\norm}[1]{\| #1 \|}\)
\( \newcommand{\inner}[2]{\langle #1, #2 \rangle}\)
\( \newcommand{\Span}{\mathrm{span}}\) \( \newcommand{\AA}{\unicode[.8,0]{x212B}}\)
\( \newcommand{\vectorA}[1]{\vec{#1}} % arrow\)
\( \newcommand{\vectorAt}[1]{\vec{\text{#1}}} % arrow\)
\( \newcommand{\vectorB}[1]{\overset { \scriptstyle \rightharpoonup} {\mathbf{#1}} } \)
\( \newcommand{\vectorC}[1]{\textbf{#1}} \)
\( \newcommand{\vectorD}[1]{\overrightarrow{#1}} \)
\( \newcommand{\vectorDt}[1]{\overrightarrow{\text{#1}}} \)
\( \newcommand{\vectE}[1]{\overset{-\!-\!\rightharpoonup}{\vphantom{a}\smash{\mathbf {#1}}}} \)
\( \newcommand{\vecs}[1]{\overset { \scriptstyle \rightharpoonup} {\mathbf{#1}} } \)
\(\newcommand{\longvect}{\overrightarrow}\)
\( \newcommand{\vecd}[1]{\overset{-\!-\!\rightharpoonup}{\vphantom{a}\smash {#1}}} \)
\(\newcommand{\avec}{\mathbf a}\) \(\newcommand{\bvec}{\mathbf b}\) \(\newcommand{\cvec}{\mathbf c}\) \(\newcommand{\dvec}{\mathbf d}\) \(\newcommand{\dtil}{\widetilde{\mathbf d}}\) \(\newcommand{\evec}{\mathbf e}\) \(\newcommand{\fvec}{\mathbf f}\) \(\newcommand{\nvec}{\mathbf n}\) \(\newcommand{\pvec}{\mathbf p}\) \(\newcommand{\qvec}{\mathbf q}\) \(\newcommand{\svec}{\mathbf s}\) \(\newcommand{\tvec}{\mathbf t}\) \(\newcommand{\uvec}{\mathbf u}\) \(\newcommand{\vvec}{\mathbf v}\) \(\newcommand{\wvec}{\mathbf w}\) \(\newcommand{\xvec}{\mathbf x}\) \(\newcommand{\yvec}{\mathbf y}\) \(\newcommand{\zvec}{\mathbf z}\) \(\newcommand{\rvec}{\mathbf r}\) \(\newcommand{\mvec}{\mathbf m}\) \(\newcommand{\zerovec}{\mathbf 0}\) \(\newcommand{\onevec}{\mathbf 1}\) \(\newcommand{\real}{\mathbb R}\) \(\newcommand{\twovec}[2]{\left[\begin{array}{r}#1 \\ #2 \end{array}\right]}\) \(\newcommand{\ctwovec}[2]{\left[\begin{array}{c}#1 \\ #2 \end{array}\right]}\) \(\newcommand{\threevec}[3]{\left[\begin{array}{r}#1 \\ #2 \\ #3 \end{array}\right]}\) \(\newcommand{\cthreevec}[3]{\left[\begin{array}{c}#1 \\ #2 \\ #3 \end{array}\right]}\) \(\newcommand{\fourvec}[4]{\left[\begin{array}{r}#1 \\ #2 \\ #3 \\ #4 \end{array}\right]}\) \(\newcommand{\cfourvec}[4]{\left[\begin{array}{c}#1 \\ #2 \\ #3 \\ #4 \end{array}\right]}\) \(\newcommand{\fivevec}[5]{\left[\begin{array}{r}#1 \\ #2 \\ #3 \\ #4 \\ #5 \\ \end{array}\right]}\) \(\newcommand{\cfivevec}[5]{\left[\begin{array}{c}#1 \\ #2 \\ #3 \\ #4 \\ #5 \\ \end{array}\right]}\) \(\newcommand{\mattwo}[4]{\left[\begin{array}{rr}#1 \amp #2 \\ #3 \amp #4 \\ \end{array}\right]}\) \(\newcommand{\laspan}[1]{\text{Span}\{#1\}}\) \(\newcommand{\bcal}{\cal B}\) \(\newcommand{\ccal}{\cal C}\) \(\newcommand{\scal}{\cal S}\) \(\newcommand{\wcal}{\cal W}\) \(\newcommand{\ecal}{\cal E}\) \(\newcommand{\coords}[2]{\left\{#1\right\}_{#2}}\) \(\newcommand{\gray}[1]{\color{gray}{#1}}\) \(\newcommand{\lgray}[1]{\color{lightgray}{#1}}\) \(\newcommand{\rank}{\operatorname{rank}}\) \(\newcommand{\row}{\text{Row}}\) \(\newcommand{\col}{\text{Col}}\) \(\renewcommand{\row}{\text{Row}}\) \(\newcommand{\nul}{\text{Nul}}\) \(\newcommand{\var}{\text{Var}}\) \(\newcommand{\corr}{\text{corr}}\) \(\newcommand{\len}[1]{\left|#1\right|}\) \(\newcommand{\bbar}{\overline{\bvec}}\) \(\newcommand{\bhat}{\widehat{\bvec}}\) \(\newcommand{\bperp}{\bvec^\perp}\) \(\newcommand{\xhat}{\widehat{\xvec}}\) \(\newcommand{\vhat}{\widehat{\vvec}}\) \(\newcommand{\uhat}{\widehat{\uvec}}\) \(\newcommand{\what}{\widehat{\wvec}}\) \(\newcommand{\Sighat}{\widehat{\Sigma}}\) \(\newcommand{\lt}{<}\) \(\newcommand{\gt}{>}\) \(\newcommand{\amp}{&}\) \(\definecolor{fillinmathshade}{gray}{0.9}\)Como comentamos en el Capítulo\(6\), los aldehídos y cetonas reaccionan con reactivos que son capaces de suministrar hidruro (por ejemplo a partir de borohidruro de sodio) o un carbanión (en forma de reactivo de Grignard) al grupo carbonilo.
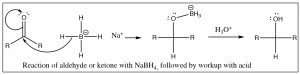
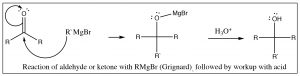
Además de los reactivos de Grignard, también se pueden generar carbaniones tratando haluros de alquilo con litio en condiciones secas. Estos reactivos de alquil litio (\(\mathrm{RLi}\)) se comportan de manera muy similar a los reactivos de Grignard, aunque son algo más reactivos.
Estas dos reacciones: la adición de hidruro (reducción) o un carbanión (dando como resultado la formación de enlaces carbono-carbono) a un carbonilo son análogas. También tienen algo más en común en que, en condiciones normales de laboratorio, no son reversibles porque invertir la reacción requeriría que el ion hidruro o carbanión sea expulsado del carbono central. Estas especies son bases muy inestables, muy fuertes. Los reactivos que los produjeron (\(\mathrm{NaBH}_{4}\),\(\mathrm{RMgX}\),\(\mathrm{RLi}\)) son reactivos especializados que no contienen iones hidruro “desnudos” o carbaniones. Si quisiéramos revertirlos, tendríamos que usar condiciones de reacción completamente diferentes que evitaran la expulsión del hidruro o carbanión de alta energía. Por ejemplo, para lograr lo contrario de la reacción de reducción, tendríamos que usar un agente oxidante (como\(\mathrm{Cr}\) (VI)) en condiciones completamente diferentes. La reducción de un grupo cetona es fundamental para las reacciones de glucólisis, en las que el piruvato (la base conjugada del ácido pirúvico [3]) se reduce a lactato (la base conjugada del ácido láctico) por\(\mathrm{NADH}\) (ver Capítulo\(6\)). Esta reacción también se puede revertir bajo diferentes condiciones (en este caso, la presencia de la enzima lactato deshidrogenasa). La glicólisis se discutirá con más detalle en el Capítulo\(9\).
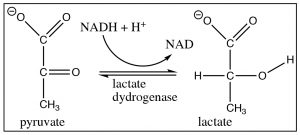
Reacción con otros carbaniones:
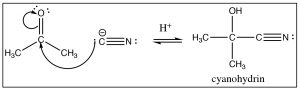
Existen otras formas de generar carbaniones: por ejemplo, los alquinos terminales son bastante ácidos (\(\mathrm{pK}_{\mathrm{a}} 22\)) y pueden ser desprotonados por amida sódica (Capítulo\(5\)). El carbanión resultante se añade al carbonilo tal como cabría esperar. Del mismo modo, el ion cianuro (\(\mathrm{CN}^{-}\)) es otra fuente de un carbono cargado negativamente. Es un buen nucleófilo, y tal como cabría esperar, se suma a los grupos carbonilo, y después de la reacción con un ácido diluido, se forma la cianhidrina resultante. Hay dos elementos a tener en cuenta aquí:
- El cianuro de sodio\(\mathrm{NaCN}\) (la forma habitual de ion cianuro) es altamente tóxico, así que no intentes esto en casa.
- El estado de oxidación del carbono en el grupo ciano es el mismo que un ácido carboxílico. Como veremos más adelante, esta reacción vendrá en muy útil. Todas estas reacciones son el resultado de una adición nucleofílica al grupo carbonilo, durante el transcurso de la cual el carbono carbonilo se rehibrida de\(\mathrm{sp}^{2}\) a\(\mathrm{sp}^{3}\).


