17.6: La corrosión
- Page ID
- 1948
\( \newcommand{\vecs}[1]{\overset { \scriptstyle \rightharpoonup} {\mathbf{#1}} } \)
\( \newcommand{\vecd}[1]{\overset{-\!-\!\rightharpoonup}{\vphantom{a}\smash {#1}}} \)
\( \newcommand{\dsum}{\displaystyle\sum\limits} \)
\( \newcommand{\dint}{\displaystyle\int\limits} \)
\( \newcommand{\dlim}{\displaystyle\lim\limits} \)
\( \newcommand{\id}{\mathrm{id}}\) \( \newcommand{\Span}{\mathrm{span}}\)
( \newcommand{\kernel}{\mathrm{null}\,}\) \( \newcommand{\range}{\mathrm{range}\,}\)
\( \newcommand{\RealPart}{\mathrm{Re}}\) \( \newcommand{\ImaginaryPart}{\mathrm{Im}}\)
\( \newcommand{\Argument}{\mathrm{Arg}}\) \( \newcommand{\norm}[1]{\| #1 \|}\)
\( \newcommand{\inner}[2]{\langle #1, #2 \rangle}\)
\( \newcommand{\Span}{\mathrm{span}}\)
\( \newcommand{\id}{\mathrm{id}}\)
\( \newcommand{\Span}{\mathrm{span}}\)
\( \newcommand{\kernel}{\mathrm{null}\,}\)
\( \newcommand{\range}{\mathrm{range}\,}\)
\( \newcommand{\RealPart}{\mathrm{Re}}\)
\( \newcommand{\ImaginaryPart}{\mathrm{Im}}\)
\( \newcommand{\Argument}{\mathrm{Arg}}\)
\( \newcommand{\norm}[1]{\| #1 \|}\)
\( \newcommand{\inner}[2]{\langle #1, #2 \rangle}\)
\( \newcommand{\Span}{\mathrm{span}}\) \( \newcommand{\AA}{\unicode[.8,0]{x212B}}\)
\( \newcommand{\vectorA}[1]{\vec{#1}} % arrow\)
\( \newcommand{\vectorAt}[1]{\vec{\text{#1}}} % arrow\)
\( \newcommand{\vectorB}[1]{\overset { \scriptstyle \rightharpoonup} {\mathbf{#1}} } \)
\( \newcommand{\vectorC}[1]{\textbf{#1}} \)
\( \newcommand{\vectorD}[1]{\overrightarrow{#1}} \)
\( \newcommand{\vectorDt}[1]{\overrightarrow{\text{#1}}} \)
\( \newcommand{\vectE}[1]{\overset{-\!-\!\rightharpoonup}{\vphantom{a}\smash{\mathbf {#1}}}} \)
\( \newcommand{\vecs}[1]{\overset { \scriptstyle \rightharpoonup} {\mathbf{#1}} } \)
\(\newcommand{\longvect}{\overrightarrow}\)
\( \newcommand{\vecd}[1]{\overset{-\!-\!\rightharpoonup}{\vphantom{a}\smash {#1}}} \)
\(\newcommand{\avec}{\mathbf a}\) \(\newcommand{\bvec}{\mathbf b}\) \(\newcommand{\cvec}{\mathbf c}\) \(\newcommand{\dvec}{\mathbf d}\) \(\newcommand{\dtil}{\widetilde{\mathbf d}}\) \(\newcommand{\evec}{\mathbf e}\) \(\newcommand{\fvec}{\mathbf f}\) \(\newcommand{\nvec}{\mathbf n}\) \(\newcommand{\pvec}{\mathbf p}\) \(\newcommand{\qvec}{\mathbf q}\) \(\newcommand{\svec}{\mathbf s}\) \(\newcommand{\tvec}{\mathbf t}\) \(\newcommand{\uvec}{\mathbf u}\) \(\newcommand{\vvec}{\mathbf v}\) \(\newcommand{\wvec}{\mathbf w}\) \(\newcommand{\xvec}{\mathbf x}\) \(\newcommand{\yvec}{\mathbf y}\) \(\newcommand{\zvec}{\mathbf z}\) \(\newcommand{\rvec}{\mathbf r}\) \(\newcommand{\mvec}{\mathbf m}\) \(\newcommand{\zerovec}{\mathbf 0}\) \(\newcommand{\onevec}{\mathbf 1}\) \(\newcommand{\real}{\mathbb R}\) \(\newcommand{\twovec}[2]{\left[\begin{array}{r}#1 \\ #2 \end{array}\right]}\) \(\newcommand{\ctwovec}[2]{\left[\begin{array}{c}#1 \\ #2 \end{array}\right]}\) \(\newcommand{\threevec}[3]{\left[\begin{array}{r}#1 \\ #2 \\ #3 \end{array}\right]}\) \(\newcommand{\cthreevec}[3]{\left[\begin{array}{c}#1 \\ #2 \\ #3 \end{array}\right]}\) \(\newcommand{\fourvec}[4]{\left[\begin{array}{r}#1 \\ #2 \\ #3 \\ #4 \end{array}\right]}\) \(\newcommand{\cfourvec}[4]{\left[\begin{array}{c}#1 \\ #2 \\ #3 \\ #4 \end{array}\right]}\) \(\newcommand{\fivevec}[5]{\left[\begin{array}{r}#1 \\ #2 \\ #3 \\ #4 \\ #5 \\ \end{array}\right]}\) \(\newcommand{\cfivevec}[5]{\left[\begin{array}{c}#1 \\ #2 \\ #3 \\ #4 \\ #5 \\ \end{array}\right]}\) \(\newcommand{\mattwo}[4]{\left[\begin{array}{rr}#1 \amp #2 \\ #3 \amp #4 \\ \end{array}\right]}\) \(\newcommand{\laspan}[1]{\text{Span}\{#1\}}\) \(\newcommand{\bcal}{\cal B}\) \(\newcommand{\ccal}{\cal C}\) \(\newcommand{\scal}{\cal S}\) \(\newcommand{\wcal}{\cal W}\) \(\newcommand{\ecal}{\cal E}\) \(\newcommand{\coords}[2]{\left\{#1\right\}_{#2}}\) \(\newcommand{\gray}[1]{\color{gray}{#1}}\) \(\newcommand{\lgray}[1]{\color{lightgray}{#1}}\) \(\newcommand{\rank}{\operatorname{rank}}\) \(\newcommand{\row}{\text{Row}}\) \(\newcommand{\col}{\text{Col}}\) \(\renewcommand{\row}{\text{Row}}\) \(\newcommand{\nul}{\text{Nul}}\) \(\newcommand{\var}{\text{Var}}\) \(\newcommand{\corr}{\text{corr}}\) \(\newcommand{\len}[1]{\left|#1\right|}\) \(\newcommand{\bbar}{\overline{\bvec}}\) \(\newcommand{\bhat}{\widehat{\bvec}}\) \(\newcommand{\bperp}{\bvec^\perp}\) \(\newcommand{\xhat}{\widehat{\xvec}}\) \(\newcommand{\vhat}{\widehat{\vvec}}\) \(\newcommand{\uhat}{\widehat{\uvec}}\) \(\newcommand{\what}{\widehat{\wvec}}\) \(\newcommand{\Sighat}{\widehat{\Sigma}}\) \(\newcommand{\lt}{<}\) \(\newcommand{\gt}{>}\) \(\newcommand{\amp}{&}\) \(\definecolor{fillinmathshade}{gray}{0.9}\)Habilidades para desarrollar
- Definir la corrosión
- Listar algunos de los métodos usados para prevenir o pausar la corrosión
La corrosión generalmente se define como la degradación de los metales debido a un proceso electroquímico. La formación de óxido en el hierro, el deslustre en la plata y la pátina azul verdosa que se desarrolla en el cobre son ejemplos de la corrosión. El costo total de la corrosión en los Estados Unidos es significativo, con estimaciones de más de medio billón de dólares al año.
Los colores cambiantes
La Estatua de la Libertad es una estatua que todos los estadounidenses reconocen. La Estatua de la Libertad se identifica fácilmente por su altura, postura y color azul verdoso único. Cuando esta estatua fue entregada por primera vez desde Francia, no aparecía verde. Era de color marrón, el color de su "piel" era cobriza. Entonces, ¿Cómo cambió de color la Estatua de la Libertad? El cambio de apariencia fue resultado directo de la corrosión. El cobre, que es el componente principal de la estatua, sufrió lentamente la oxidación del aire. Las reacciones de oxidación-reducción del cobre metálico en el medio ambiente ocurren en varios pasos. El cobre metálico se oxida a óxido de cobre (I) (\(\ce{Cu_2O}\)), que es rojo, y luego a óxido de cobre (II), que es negro.
\[\ce{2Cu}_{(s)} +\ce{½O}_{2(g)} \rightarrow \underset{\text{red}}{\ce{Cu2O}_{(s)}} \label{\(\PageIndex{1}\)}\]
\[\ce{Cu2O}_{(s)} +\ce{½O}_{2(g)}\rightarrow \underset{\text{black}}{\ce{2CuO}_{(s)}} \label{\(\PageIndex{2}\)}\]
El carbón, que a veces tenía un alto contenido de azufre, se quemó extensamente a principios del siglo pasado. Como resultado, el trióxido de azufre, el dióxido de carbono y el agua reaccionaron con \(\ce{CuO}\).
\[\ce{2CuO}_{(s)}+\ce{CO}_{2(g)} + \ce{H_2O}_{(l)} \rightarrow \underset{\text{green}}{\ce{Cu_2CO_3(OH)}_{2(s)}} \label{\(\PageIndex{3}\)}\]
\[\ce{3CuO}_{(s)}+\ce{2CO}_{2(g)}+\ce{H_2O}_{(l)} \rightarrow \underset{\text{blue}}{\ce{Cu_2(CO_3)_2(OH)}_{2(s)}} \label{\(\PageIndex{4}\)}\]
\[\ce{4CuO}_{(s)}+\ce{SO}_{3(g)}+\ce{3H_2O}_{(l)} \rightarrow \underset{\text{green}}{\ce{Cu_4SO_4(OH)}_{6(s)}} \label{\(\PageIndex{5}\)}\]
Estos tres compuestos son responsables por la característica pátina azul verdosa que se ve hoy. Afortunadamente, la formación de la pátina hizo una capa protectora en la superficie, evitando más corrosión de la “piel” de cobre. La formación de la capa protectora es una forma de pasivación, que se analiza con más detalle en un capítulo que sigue.

Quizás el ejemplo más familiar de la corrosión es la formación del óxido en el hierro. El hierro se oxida cuando está expuesto al oxígeno y al agua. Los pasos principales en la oxidación del hierro parecen involucrar lo siguiente. Una vez expuesto a la atmósfera, el hierro se oxida rápidamente.
\[\textrm{anode: }\ce{Fe}_{(s)} \rightarrow \ce{Fe^{2+}}_{(aq)}+\ce{2e^-}\;\;\; E^\circ_{\ce{Fe^{2+}/Fe}}=\mathrm{−0.44\: V}\]
Los electrones reducen el oxígeno del aire en soluciones ácidas.
\[\textrm{cathode: }\ce{O}_{2(g)}+\ce{4H^+}_{(aq)}+\ce{4e^-} \rightarrow \ce{2H_2O}_{(l)}\;\; E^\circ_{\ce{O_2/O_2}}=\mathrm{+1.23\; V}\]
Lo que llamamos óxido es el óxido de hierro (III) hidratado, que se forma cuando los iones de hierro (II) reaccionan más con el oxígeno.
\[\ce{4Fe^{2+}}_{(aq)}+\ce{O}_{2(g)}+(4+2x)\ce{H_2O}_{(l)} \rightarrow \ce{2Fe_2O_3} \cdot x\ce{H_2O}_{(s)}+\ce{8H^+}_{(aq)}\]
El número de moléculas de agua puede variar, por eso está representado por x. Diferente a la pátina sobre el cobre, la formación del óxido no crea una capa protectora y permite que la corrosión del hierro continúe a medida que el óxido se desprende y expone el hierro fresco a la atmósfera.
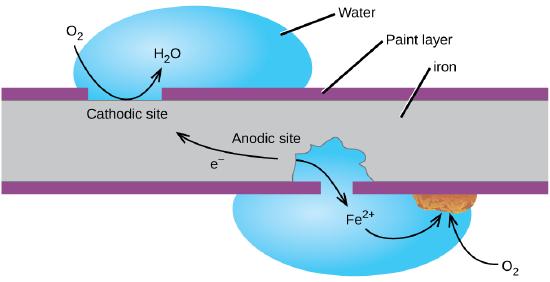
Una forma de evitar que el hierro se corroa es mantenerlo pintado. La capa de pintura evita que el agua y el oxígeno, que son necesarios para la formación del óxido, entren en contacto con el hierro. Mientras la pintura permanezca intacta, el hierro está protegido de la corrosión.
Otras estrategias incluyen la aleación del hierro con otros metales. Por ejemplo, el acero inoxidable es principalmente hierro con un poco de cromo. El cromo se tiende a acumular cerca de la superficie, donde forma una capa de óxido que protege el hierro.
El hierro zincado o galvanizado usa una estrategia diferente. El zinc se oxida más fácilmente que el hierro porque el zinc tiene un potencial de reducción más pequeño. Ya que el zinc tiene un potencial de reducción más pequeña, es un metal más activo. Por lo tanto, incluso si se raya el recubrimiento de zinc, el zinc se oxidará antes que el hierro. Esto sugiere que este enfoque debería funcionar con otros metales activos.

Otra forma importante de proteger el metal es convertirlo en el cátodo en una celda galvánica. Esta es una protección catódica y se puede usar para otros metales además del hierro. Por ejemplo, la oxidación de los tanques y tuberías de almacenamiento de hierro subterráneos se puede prevenir o reducir en gran medida cuando se conectan a un metal más activo como el zinc o el magnesio. También se usa para proteger las partes metálicas de los calentadores de agua. Los metales más activos (potencial de reducción más pequeño) se llaman los ánodos de sacrificio porque cuando se gastan se corroen (oxidan) en el ánodo. El metal que se protege sirve como el cátodo y, por lo tanto, no se oxida (corroe). Cuando los ánodos se controlan adecuadamente y se reemplazan periódicamente, la vida útil del tanque de almacenamiento de hierro puede prolongarse considerablemente.
Resumen
La corrosión es la degradación de un metal causada por un proceso electroquímico. Cada año se gastan grandes sumas de dinero para reparar los efectos de la corrosión. Algunos metales, como el aluminio y el cobre, producen una capa protectora cuando se corroen en el aire. La capa delgada que se forma en la superficie del metal evita que el oxígeno entre en contacto con más átomos del metal y “protege” el metal restante de más corrosión. El hierro se corroe (forma óxido) cuando está expuesto al agua y al oxígeno. El óxido que se forma en el metal de hierro se desprende, exponiendo el metal fresco, que también se corroe. Una forma de prevenir o ralentizar la corrosión es recubriendo el metal. El revestimiento evita que el agua y el oxígeno entren en contacto con el metal. La pintura u otros recubrimientos ralentizan la corrosión, pero no son efectivos una vez que se rayan. El hierro cincado o galvanizado aprovecha el hecho de que el zinc tiene más probabilidades de oxidarse que el hierro. Mientras el recubrimiento permanezca, aunque se raye, el zinc se oxidará antes que el hierro. Otro método para proteger los metales es la protección catódica. En este método, un metal económico y fácilmente oxidable, a veces el zinc o el magnesio (el ánodo de sacrificio), se conecta eléctricamente al metal que se debe proteger. El metal más activo es el ánodo de sacrificio y es el ánodo en una celda galvánica. El metal "protegido" es el cátodo y permanece sin oxidarse. Una ventaja de la protección catódica es que el ánodo de sacrificio se puede monitorear y reemplazar si es necesario.
Glosario
- protección catódica
- método de protección del metal usando un ánodo de sacrificio haciendo el metal que necesita proteger el cátodo, evitando así su oxidación
- la corrosión
- degradación del metal a través de un proceso electroquímico
- hierro galvanizado
- método para proteger el hierro cubriéndolo con zinc, que se oxidará antes que el hierro; hierro cincado
- ánodo de sacrificio
- metal más activo y económico usado como el ánodo en la protección catódica; frecuentemente hecho del magnesio o el zinc
Contribuyentes
Paul Flowers (Universidad de Carolina del Norte - Pembroke), Klaus Theopold (Universidad de Delaware) y Richard Langley (Stephen F. Austin Universidad del Estado) con autores contribuyentes. Contenido del libro de texto producido por la Universidad de OpenStax tiene licencia de Atribución de Creative Commons Licencia 4.0 licencia. Descarge gratis en http://cnx.org/contents/85abf193-2bd...a7ac8df6@9.110)."
Ana Martinez (amartinez02@saintmarys.edu) contribuyó a la traducción de este texto.


